Psoríase: o que a pele mostra, e o que a ciência explica por trás disso?
Quem convive com psoríase costuma descrever a mesma cena: a pele começa a descamar, surgem placas avermelhadas, às vezes coçam, às vezes doem. Em muitos casos, aparecem e desaparecem em ciclos que parecem imprevisíveis. Mas o que a medicina já entende hoje é que a psoríase não começa na pele, ela se manifesta nela.
Ela é considerada uma das doenças inflamatórias cutâneas mais comuns, com importante componente genético presente em cerca de 30% dos casos — e pode surgir em qualquer fase da vida, sendo mais frequente entre os 30 e 40 anos. Apesar de suas manifestações visíveis, é importante reforçar: a psoríase não é contagiosa, embora ainda seja frequentemente cercada por estigmas sociais.
Estima-se que milhões de pessoas convivam com a doença no mundo, o que reforça não apenas sua relevância clínica, mas também o impacto em saúde pública.
Pela aparência, muitas vezes pode ser confundida com outras condições dermatológicas, como dermatites. No entanto, existem diferenças importantes: enquanto dermatites tendem a apresentar lesões mais úmidas e, em fases iniciais, pequenas vesículas, a psoríase se caracteriza por placas mais secas, espessas e descamativas, com base avermelhada. Ao coçar, a pele costuma descamar ainda mais, revelando esse padrão típico.
A psoríase é uma doença inflamatória crônica, imunomediada, em que o sistema imune passa a funcionar de forma desregulada, mantendo um estado inflamatório persistente mesmo sem um agente externo claro (Lowes et al., 2014).
Na prática, isso significa que o organismo passa a reagir como se estivesse constantemente sob ameaça, mantendo a inflamação ativa de forma contínua.
Para entender isso, vale imaginar como a pele funciona em condições normais.
Em uma pele saudável, as células da epiderme (os queratinócitos) seguem um ciclo organizado de renovação. Elas se formam nas camadas mais profundas, amadurecem ao longo de aproximadamente 28 dias e chegam à superfície formando uma barreira protetora estável.
Na psoríase, esse ciclo perde o ritmo.
Esse descompasso acontece porque o organismo passa a emitir sinais inflamatórios como se houvesse uma lesão constante a ser reparada. É como se a pele estivesse em um estado contínuo de “regeneração”, mesmo sem necessidade.
Esse fenômeno é central para entender a doença: não se trata apenas de crescimento acelerado, mas de crescimento desorganizado e sem controle adequado.
As células passam a se multiplicar em poucos dias, sem tempo suficiente para maturação adequada. Sobem rapidamente para a superfície ainda imaturas e se acumulam, formando as placas espessas e descamativas características da doença.
Mas essa aceleração não acontece sozinha.
Ela é sustentada por um processo inflamatório contínuo. Células do sistema imune, especialmente linfócitos T das vias Th1 e Th17, passam a liberar citocinas como TNF-α, IL-17 e IL-23, ou seja, moléculas que funcionam como amplificadores da inflamação e, ao mesmo tempo, estimulam ainda mais a proliferação dos queratinócitos.
Essas citocinas funcionam como verdadeiros “interruptores biológicos”, mantendo o sistema ligado continuamente.
Em termos mais simples, essas citocinas funcionam como “mensageiros de alerta”, dizendo para a pele continuar inflamada e produzir mais células, mesmo quando isso já não é necessário.
Cria-se um ciclo difícil de interromper:
a inflamação acelera a renovação celular, e a renovação celular perpetua a inflamação.
A pele entra em um estado de atividade constante.
Essa dinâmica fica mais clara quando observamos a estrutura da pele em psoríase. Essa leitura integrada é importante porque mostra que não existe um único ponto de origem da doença, mas sim um sistema em desequilíbrio.
Figura 1. Fisiopatologia da psoríase
Representação das alterações celulares e inflamatórias, incluindo ativação imune, dilatação vascular e proliferação queratinocitária.
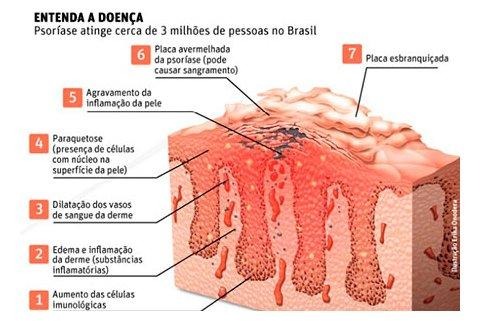
Ao olhar a figura, é possível acompanhar esse processo quase como uma sequência: o aumento de células imunológicas na derme inicia a inflamação; mediadores inflamatórios são liberados; os vasos sanguíneos se dilatam, o que explica a vermelhidão e, ao mesmo tempo, a epiderme se espessa devido à proliferação acelerada das células. Na superfície, o acúmulo celular se transforma em descamação visível.
Essa visualização ajuda a entender que a psoríase não é um problema superficial. Ela começa em camadas mais profundas da pele e envolve múltiplos sistemas ao mesmo tempo imunológico, vascular e celular:
- Aumento das células imunológicas
O sistema imune fica hiperativo e envia sinais inflamatórios constantes. - Inflamação da derme
Substâncias inflamatórias são liberadas, gerando edema e ativação celular. - Dilatação dos vasos sanguíneos
Isso explica a vermelhidão característica das lesões. - Alteração dos queratinócitos
As células da pele passam a se multiplicar rapidamente e de forma desorganizada. - Inflamação contínua
O ciclo inflamatório se mantém ativo, sem resolução. - Formação das placas
O acúmulo de células gera espessamento da pele. - Descamação visível
As placas se tornam esbranquiçadas e descamativas — sinal clássico da doença.
Mas talvez o ponto mais importante seja perceber que isso não é uma sequência linear. É um ciclo que se retroalimenta.
E é por isso que a psoríase não é apenas uma condição estética ou localizada.
Hoje já se sabe que ela está associada a um estado inflamatório sistêmico. Pacientes com psoríase apresentam maior risco de desenvolver síndrome metabólica, doenças cardiovasculares e alterações metabólicas importantes.
Isso significa que a inflamação não está restrita à pele. Ela circula pelo organismo, afetando outros sistemas e contribuindo para doenças crônicas. Além disso, o impacto vai além do biológico. Esse impacto emocional, muitas vezes silencioso, também atua como fator de agravamento, criando um ciclo entre pele e sistema nervoso.
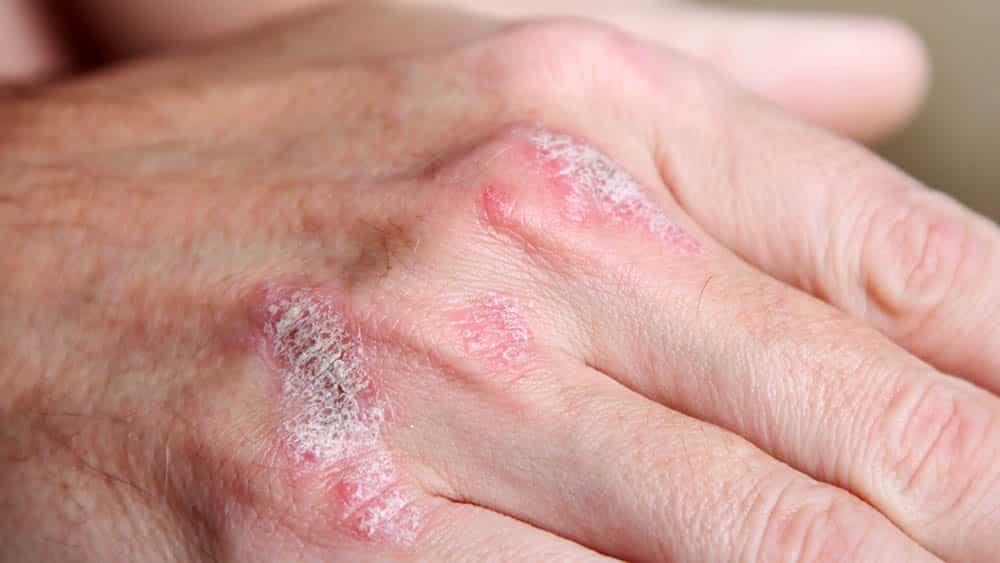
A presença de lesões visíveis como mostra a Figura 2, recorrentes e muitas vezes imprevisíveis pode afetar diretamente a qualidade de vida, com aumento de ansiedade, estresse e sintomas depressivos.
Figura 2: Lesões da pele
As imagens clínicas ajudam a reconhecer o padrão das lesões: placas bem delimitadas, avermelhadas e recobertas por escamas esbranquiçadas, frequentemente localizadas em áreas de atrito como cotovelos, joelhos e couro cabeludo.
E esses fatores, por sua vez, também influenciam a doença.
O estresse crônico, por exemplo, é reconhecido como um dos principais gatilhos de exacerbação. Ele atua modulando o sistema imune e favorecendo a manutenção do estado inflamatório.
O mesmo acontece com o consumo de álcool. Embora não seja causa direta da psoríase, o álcool está associado ao agravamento das lesões. Ele pode intensificar a inflamação sistêmica, interferir na função de barreira da pele e reduzir a resposta ao tratamento, além de impactar negativamente o comportamento do paciente em relação ao cuidado contínuo.
Outros fatores também podem atuar como gatilhos, como infecções, traumas na pele, tabagismo e uso de determinadas medicações, como o lítio. Quando juntamos todos esses fatores imunológicos, celulares, metabólicos e comportamentais fica mais claro que a psoríase não é apenas um excesso de inflamação.
Ela é, sobretudo, uma falha de regulação.
O problema não é apenas a inflamação em si, mas a incapacidade do organismo de desligá-la. O organismo perde a capacidade de equilibrar sinais que, em condições normais, seriam controlados. A inflamação não é interrompida. A renovação celular não desacelera. O sistema permanece ativado.
E é justamente esse ponto que começa a mudar a forma como a ciência pensa o tratamento.
Porque, se o problema é de regulação, talvez não seja suficiente apenas bloquear a inflamação. Talvez seja necessário entender quais sistemas do próprio organismo participam desse equilíbrio e como eles podem ser modulados. Entre esses sistemas, um tem ganhado destaque nos últimos anos: o sistema endocanabinoide da pele.
Mas antes de avançar, vale guardar uma ideia central:
A psoríase não começa na superfície ela é a expressão visível de um sistema que perdeu o controle.
Se o problema é sistêmico, por que tratamos só a superfície?
Os tratamentos convencionais como: corticoides tópicos, imunossupressores e terapias biológicas têm como objetivo principal reduzir a inflamação. E, de fato, muitos são eficazes.
Mas existe uma limitação importante: eles atuam predominantemente suprimindo a resposta inflamatória, sem necessariamente restaurar os mecanismos fisiológicos de equilíbrio da pele.
Isso significa que, em muitos casos, o controle depende do uso contínuo e, quando interrompido, a inflamação pode retornar justamente porque o sistema que regula a pele permanece desajustado.
É nesse contexto que novas abordagens terapêuticas começam a ser investigadas.
A pele não é passiva: ela responde
Durante muito tempo, a pele foi considerada apenas uma barreira física. Hoje sabemos que ela é um órgão altamente ativo, capaz de produzir mediadores inflamatórios, interagir com o sistema imune e regular sua própria homeostase.
Além disso, a pele possui comunicação direta com o sistema nervoso e imunológico, funcionando como um verdadeiro órgão neuroimunoendócrino.
E é aqui que entra um conceito central da biologia moderna:
O SISTEMA ENDOCANABINOIDE: SEC
O sistema que regula a pele e que poucos conhecem.
A pele possui receptores e vias bioquímicas que fazem parte do chamado sistema endocanabinoide (SEC), é uma rede de sinalização envolvida na regulação de inflamação, proliferação celular, dor e resposta imune.
Esse sistema é composto por:
- receptores CB1 e CB2
- endocanabinoides produzidos pelo próprio organismo
- enzimas responsáveis pela sua síntese e degradação
Mais recentemente, esse conceito foi ampliado para o chamado endocannabinoidoma, que inclui outros alvos moleculares, como canais TRP e receptores nucleares PPAR-γ, ampliando a complexidade e o alcance funcional desse sistema.
Figura 3 – Visão geral do sistema endocanabinoide cutâneo
Representação esquemática dos principais elementos do sistema endocanabinoide nos compartimentos celulares da pele. Fonte: MONTAGNER, Patrícia; DE SALAS-QUIROGA, Adán. Tratado de Medicina Endocanabinoide.1. ed. WeCann Endocannabinoid Global Academy, 2023.
A Figura 3 não apenas mostra a presença desses componentes, mas evidencia que o SEC atua como um sistema de integração conectando resposta imune, atividade celular e percepção sensorial na pele. O SEC está distribuído em diferentes estruturas da pele e como ele atua de forma integrada na regulação de funções essenciais.
No centro da figura estão os principais endocanabinoides produzidos pelo próprio organismo como a anandamida (AEA) e o 2-AG que funcionam como moléculas sinalizadoras. Eles são liberados localmente e interagem com receptores presentes em múltiplos componentes da pele.
Esses receptores, especialmente CB1 e CB2, não estão restritos a uma única região. Eles aparecem em células imunológicas, na epiderme, nas glândulas sebáceas, nos folículos pilosos e até em terminações nervosas sensoriais. Isso ajuda a explicar por que o sistema endocanabinoide participa de processos tão diversos ao mesmo tempo.
Ao observar as setas da figura, é possível entender essa ação de forma mais funcional.
Na epiderme, a ativação desses receptores está associada à redução da proliferação celular e ao controle da diferenciação dos queratinócitos dois pontos diretamente envolvidos na fisiopatologia da psoríase.
Nas células imunológicas, o sistema atua modulando a inflamação, reduzindo a liberação de mediadores inflamatórios. Isso é particularmente relevante em doenças inflamatórias crônicas, onde essa resposta se encontra exacerbada.
Nas terminações nervosas, a ativação do SEC está relacionada à diminuição da dor e do prurido, sintomas frequentemente relatados por pacientes.
Já nas glândulas sebáceas e nos folículos pilosos, observa-se influência na produção lipídica, crescimento capilar e apoptose celular mostrando que o sistema não atua apenas na inflamação, mas também na homeostase geral da pele.
Outro ponto importante é a presença de outros receptores além dos clássicos CB1 e CB2. A figura 3 destaca canais TRP e receptores como PPAR-γ, que fazem parte do chamado endocannabinoidoma uma rede expandida que amplia ainda mais o alcance biológico desse sistema.
O que essa imagem revela, de forma integrada, é que o SEC não atua de maneira isolada ou pontual.
Ele funciona como um regulador central da pele.
Não é um sistema que “ativa” ou “desativa” funções é um sistema que ajusta, equilibra e modula respostas.
E é justamente essa capacidade de regulação que começa a chamar atenção da ciência quando pensamos em condições como a psoríase, onde o principal problema não é a ausência de resposta, mas o excesso dela.
E onde entra a cannabis?
Se o organismo já possui um sistema preparado para responder a essas moléculas, a pergunta muda completamente.
Não se trata apenas de “usar cannabis na pele”.
Mas sim: como os compostos da cannabis interagem com um sistema que já existe no corpo?
Os canabinoides, como o canabidiol (CBD) e o canabigerol (CBG), possuem estrutura química capaz de interagir com esses receptores e modular suas funções.
Eles não criam um efeito artificial.
Eles modulam um sistema fisiológico que está desregulado, como ocorre na psoríase.
Estudos in vitro e clínicos mostram que canabinoides conseguem modular diretamente vias envolvidas na psoríase, incluindo a proliferação queratinocitária e a produção de citocinas inflamatórias.
CBD e CBG: moléculas diferentes, respostas complementares.
Dentro desse sistema mais complexo, cada canabinoide exerce um papel distinto.
O canabidiol (CBD) é hoje o composto mais estudado na dermatologia. Ele atua como modulador multifuncional, com efeitos bem descritos em diferentes níveis da fisiopatologia da pele:
- reduz citocinas pró-inflamatórias como TNF-α, IL-6 e IL-1β
- inibe a hiperproliferação de queratinócitos
- exerce ação antioxidante, reduzindo o estresse oxidativo celular
- modula receptores como TRPV1 e PPAR-γ, envolvidos na inflamação e diferenciação celular
Na prática, isso significa que o CBD atua diretamente em dois pilares centrais da psoríase: inflamação e renovação celular desregulada.
Já o canabigerol (CBG), embora menos estudado em ensaios clínicos, apresenta um perfil farmacológico extremamente interessante em estudos pré-clínicos.
Ele demonstra:
- forte afinidade por receptores CB2 (relacionados à resposta imune)
- modulação de canais TRP envolvidos em dor e inflamação
- ativação de PPAR-γ, com impacto na regulação gênica inflamatória
- efeito antimicrobiano relevante na pele
Esse conjunto de ações posiciona o CBG como um potencial modulador mais direto da inflamação imune cutânea.
Mas, para que isso faça sentido fora do laboratório, é importante traduzir essa interação para uma linguagem mais próxima da realidade do leitor.
Uma forma didática de entender é pensar nos canabinoides como funções diferentes dentro de um mesmo sistema regulador.
O CBD atua principalmente como um mediador.
Ele não “força” uma resposta específica ele ajuda o organismo a encontrar equilíbrio. Em termos biológicos, reduz excessos: diminui inflamação exagerada, controla a proliferação celular e modula sinais que estão desregulados, de maneira simples.
o CBD funciona como alguém que organiza o ambiente quando tudo está caótico, ou seja ele não cria novas regras, mas ajuda o sistema a voltar ao equilíbrio.
Já o CBG tem um perfil mais ativo em algumas vias, especialmente relacionadas à resposta imune.
Ele pode ser entendido como um modulador mais direto ou “pacificador ativo”, atuando em receptores como CB2 e canais inflamatórios, ajudando a conter respostas imunes exacerbadas e, em alguns contextos, exercendo também efeito antimicrobiano.
De forma simples, existem canabinoides com respostas diferentes:
- enquanto o CBD organiza o ambiente, o CBG atua diretamente em focos específicos do problema ajudando a “conter o conflito” onde ele está acontecendo.
Esses efeitos já foram demonstrados em modelos celulares de queratinócitos humanos, onde o CBD foi capaz de normalizar padrões de proliferação e diferenciação.
POR QUE ISSO IMPORTA?
Quando utilizados em conjunto em formulações chamadas de blends esses canabinoides não competem entre si. Pelo contrário, eles se complementam.
- o CBD regula o sistema como um todo
- o CBG atua de forma mais direcionada em vias inflamatórias
Essa complementaridade permite uma atuação mais ampla e, potencialmente, mais eficaz sobre condições complexas como a psoríase, que não depende de um único mecanismo, mas de uma rede de processos desregulados.
“Na pele, os canabinoides não funcionam como um único ativo isolado, mas como um sistema de regulação: enquanto o CBD ajuda a restaurar o equilíbrio, o CBG atua diretamente na contenção da inflamação.” Dra. Lih Vitória
Quando os canabinoides atuam juntos: o conceito de “blend”
Se cada molécula tem um papel, surge uma pergunta natural:
faz sentido utilizar apenas um canabinoide isolado?
A ciência mais recente aponta que não necessariamente.
A cannabis funciona como um sistema farmacológico integrado. Quando combinados, canabinoides como CBD e CBG podem atuar de forma complementar, atingindo múltiplas vias simultaneamente.
Esse fenômeno é frequentemente associado ao chamado efeito entourage, no qual diferentes compostos da planta incluindo terpenos, flavonoides, canabinoides ácidos modulam e potencializam seus efeitos biológicos.
No contexto da pele, isso significa:
- maior amplitude de ação anti-inflamatória
- modulação simultânea de diferentes receptores
- potencial efeito mais equilibrado sobre proliferação celular e resposta imune
Em termos simples:
não é apenas a intensidade da ação que importa, mas a forma como diferentes vias são reguladas ao mesmo tempo.
E por que o uso tópico faz sentido na regulação?
Se esses compostos atuam diretamente em receptores presentes na pele, a via de administração se torna um fator decisivo.
O uso tópico permite:
- ação localizada diretamente no tecido afetado
- menor exposição sistêmica
- maior interação com o sistema endocanabinoide cutâneo
Além disso, evita um problema importante observado em vias orais e sublinguais para essas condições: a baixa biodisponibilidade para atingir a pele de forma eficaz.
No entanto, existe um desafio farmacotécnico relevante.
Canabinoides como o CBD e o CBG são moléculas lipofílicas, o que dificulta sua penetração através da barreira cutânea.
Por isso, a eficácia do uso tópico não depende apenas da substância mas da tecnologia envolvida na formulação.
Estratégias como:
- nanoemulsões
- lipossomas
- sistemas de liberação controlada
têm sido estudadas para aumentar a permeação e garantir que essas moléculas alcancem camadas mais profundas da pele, onde exercem seus efeitos.
O que isso muda na forma de pensar tratamento?
Esse conjunto de evidências nos leva a uma mudança importante de perspectiva.
Não estamos mais falando apenas de aplicar um ativo na pele.
Estamos falando de:
- modular um sistema biológico complexo
- utilizar combinações moleculares com ações complementares
- e considerar a tecnologia farmacêutica como parte essencial da resposta clínica
E é justamente essa combinação entre canabinoide + sinergia + formulação adequada que começa a explicar por que os resultados clínicos observados com CBD tópico não são apenas pontuais, mas biologicamente plausíveis.
Quando a teoria encontra a prática: A Aplicação da Cannabis na pele.
Mas o que acontece quando essa lógica de modular o sistema sai do campo teórico e chega até o paciente?
Nos últimos anos, alguns estudos começaram a testar exatamente isso: a aplicação tópica de canabinoides em doenças inflamatórias da pele, como a psoríase. E, ainda que seja um campo em desenvolvimento, os resultados começam a apontar na mesma direção.
Um dos estudos clínicos mais relevantes foi publicado em 2022 no Journal of the European Academy of Dermatology and Venereology. Trata-se de um ensaio clínico randomizado, duplo-cego e controlado por placebo, conduzido com 51 pacientes com psoríase em placas leve, utilizando uma pomada com 2,5% de canabidiol (CBD) ao longo de 12 semanas (HINZ et al., 2022).
O desenho do estudo chama atenção: modelo “split-body”. Cada paciente aplicava CBD em uma lesão e placebo em outra. Isso permite uma comparação direta no mesmo organismo, reduzindo variações individuais. Os resultados foram consistentes.
Houve redução significativa do escore clínico de psoríase (LPSI), melhora da descamação já nas primeiras semanas e uma tendência de redução da área das lesões tratadas com CBD. Além disso, o tratamento foi bem tolerado, sem efeitos adversos relevantes.
Mas o dado mais interessante não está apenas na melhora clínica.
Os autores descrevem que o CBD atua diretamente em mecanismos centrais da doença, incluindo a inibição da proliferação de queratinócitos e a modulação de citocinas inflamatórias como TNF-α e interleucinas vias que sustentam a inflamação crônica da psoríase. A Figura 4 mostra as comparações entre lesão tratada com CBD e placebo.
Figura 4 – Evolução clínica comparativa entre lesão tratada com canabidiol (CBD) e placebo ao longo de 12 semanas.
Ao observar a figura, o que se vê não é apenas uma melhora estética é uma mudança de comportamento da pele ao longo do tempo.
- Na linha superior (CBD), a lesão inicia com placas espessas e descamativas e evolui progressivamente para uma superfície mais homogênea, com redução visível da inflamação e da descamação já nas primeiras semanas.
Esse padrão temporal é importante. A melhora não ocorre apenas no final do tratamento, mas de forma gradual o que sugere uma modulação contínua dos processos inflamatórios e da renovação celular.
Já na área tratada com placebo, embora exista alguma variação natural da lesão, a resposta é menos consistente e menos intensa ao longo das semanas. Esse tipo de comparação, no mesmo paciente, reduz interferências externas e reforça que o efeito observado está associado à intervenção.
Outro ponto relevante é que a melhora visível acompanha aquilo que já foi descrito nos mecanismos moleculares:
- redução da inflamação
- menor descamação (ligada à proliferação celular)
- reorganização da superfície cutânea
Ou seja, a imagem traduz visualmente o que a ciência já vem sugerindo.
- Não é apenas uma pele “menos vermelha”.
- É uma pele que está voltando a um padrão mais equilibrado de funcionamento.
Antes mesmo desse ensaio controlado, um estudo clínico conduzido por Palmieri et al. (2019), publicado na revista Clinical Terapeutics, já havia observado efeitos semelhantes com o uso tópico de CBD em pacientes com doenças inflamatórias da pele. Ao longo de três meses de aplicação, foram observadas melhora da hidratação cutânea, redução do prurido e diminuição da inflamação, sem registro de efeitos adversos significativos (PALMIERI et al., 2019).
Mas talvez o ponto mais interessante desse estudo esteja naquilo que conseguimos observar diretamente nas imagens clínicas, como ilustrado nas Figuras 5-7, que apresentam comparações antes e depois do tratamento.
Figuras 5A–5B, 6A–6B e 7A–7B- Evolução clínica de alterações cutâneas antes e após tratamento tópico com canabidiol (CBD).
As imagens apresentam comparações antes (A) e após (B) três meses consecutivos de uso da formulação tópica (CBD:THC), aplicada duas vezes ao dia. Observam-se lentigos solares na perna direita (Figuras 5A–5B) e no braço direito (Figuras 6A–6B) de paciente do sexo feminino, 73 anos, além de cicatriz pós-cirúrgica por remoção de cisto em paciente do sexo masculino, 78 anos (Figuras 7A–7B). Nota-se melhora do aspecto cutâneo, com redução de irregularidades, inflamação e melhor organização da superfície da pele.
Fonte: PALMIERI et al., 2019 (Clinical Therapeutics).
Ao observar essas imagens, o que chama atenção não é apenas a melhora pontual de uma lesão, mas a resposta global da pele ao longo do tempo.
Há uma redução visível da inflamação, melhora da textura cutânea e, no caso da cicatriz, uma reorganização do tecido sinais que vão além de um efeito superficial.
Esse tipo de resultado ajuda a entender um ponto importante.
O CBD não atua apenas “secando” a lesão ou reduzindo temporariamente a inflamação. Ele parece interferir em processos mais amplos da pele, como:
- regulação inflamatória
- equilíbrio da função de barreira
- renovação e organização celular
Em outras palavras, a pele não apenas melhora ela muda a forma como responde, ou seja modula respostas inflamatórias. Mesmo não sendo um estudo controlado por placebo, os achados de Palmieri são relevantes porque mostram algo que começa a se repetir em outros trabalhos: a resposta não é isolada, nem imediatista, ela é progressiva, integrada e funcional.
E é justamente esse padrão que começa a sustentar a ideia de que os canabinoides não atuam como agentes pontuais, mas como moduladores da fisiologia cutânea.
Ela melhora como um todo: hidratação, inflamação, conforto.
Esse tipo de resposta sugere um efeito funcional, mais próximo de modulação do que de simples supressão de sintomas.
Quando olhamos para os estudos experimentais, essa resposta começa a fazer ainda mais sentido.
Quando avançamos da observação clínica para o nível celular, os dados ajudam a sustentar aquilo que já começa a ser visto na prática.
Um estudo clássico publicado no Journal of Dermatological Science demonstrou que diferentes canabinoides, incluindo o canabidiol (CBD) e o canabigerol (CBG), são capazes de inibir a proliferação de queratinócitos humanos um dos processos centrais envolvidos na formação das placas psoriáticas (WILKINSON; WILLIAMSON, 2007).
Na psoríase, esse processo encontra-se desregulado. Os queratinócitos passam a se multiplicar de forma acelerada e desorganizada, contribuindo diretamente para o espessamento da pele e a descamação característica da doença.
O que esse estudo mostra é que os canabinoides conseguem atuar exatamente nesse ponto.
Figura 8. Efeito do canabidiol (CBD) e do canabigerol (CBG) na proliferação de queratinócitos humanos.
A Figura 8 avalia curvas dose-resposta após 72 horas de exposição aos fitocanabinoides demonstram redução significativa da proliferação celular, de forma dependente da concentração. Os dados evidenciam o potencial antiproliferativo dessas moléculas sobre queratinócitos, processo diretamente relacionado à fisiopatologia da psoríase. Fonte: Adaptado de WILKINSON; WILLIAMSON, 2007 (Journal of Dermatological Science).
Ao observar a figura, fica evidente que o efeito não é pontual.
A inibição da proliferação ocorre de forma progressiva, conforme aumenta a concentração dos canabinoides, indicando uma resposta biológica consistente.
Esse dado é particularmente relevante porque conecta diretamente o mecanismo ao quadro clínico. Se na psoríase há uma multiplicação acelerada das células da pele, a capacidade de reduzir essa proliferação sugere um efeito que vai além do controle da inflamação atuando também na base estrutural da formação das lesões.
Outro ponto importante descrito pelos autores é que esse efeito não depende exclusivamente dos receptores clássicos CB1 e CB2.
Isso indica a participação de outras vias, como canais TRP e receptores nucleares, reforçando a ideia de que os canabinoides atuam em uma rede de regulação mais ampla o que hoje entendemos como parte do endocannabinoidoma.
Ao olhar para o conjunto das evidências disponíveis, o que emerge não é uma promessa isolada, mas uma linha de investigação consistente. Os fitocanabinoides, um dos principais compostos da Cannabis sativa, vem sendo estudado por sua capacidade de interagir com múltiplos alvos moleculares presentes na pele desde receptores envolvidos na inflamação até vias relacionadas à regeneração e ao equilíbrio da barreira cutânea. Como aponta a revisão publicada na Phytochemistry Reviews (ATTI et al., 2023), os dados pré-clínicos já sustentam esse potencial, enquanto os estudos clínicos ainda em expansão começam a mostrar efeitos em condições como psoríase, dermatite e acne, além de impactos na hidratação, elasticidade e proteção da pele. A Figura 9 mostra o esquema dos receptores modulados pelo canabidiol (CBD) e sua distribuição na pele.
Representação esquemática dos principais alvos moleculares do CBD, incluindo receptores canabinoides (CB1 e CB2), canais TRP e receptores nucleares como PPAR-γ, distribuídos em diferentes estruturas cutâneas, como epiderme, derme, células imunológicas e terminações nervosas. A imagem ilustra a complexidade da interação entre o CBD e o sistema endocanabinoide expandido (endocannabinoidoma).
Fonte: Adaptado de ATTI et al., 2023 (Phytochemistry Reviews). Criado com BioRender.
Ao observar todos esses mecanismos, fica mais fácil entender por que reduzir a cannabis a “gotinhas de CBD” é uma simplificação que não acompanha o que a ciência já mostra hoje.
Os canabinoides não atuam em um único receptor, nem segue uma única via. Eles interagem com uma rede de alvos distribuídos pela pele receptores canabinoides clássicos, canais iônicos como os TRP, receptores nucleares como o PPAR-γ todos envolvidos em processos essenciais como inflamação, dor, proliferação celular e função de barreira.
A pele, nesse contexto, não é apenas um local de aplicação.
Ela é um sistema biologicamente ativo, com capacidade de resposta e autorregulação.
E é justamente nessa interface que a cannabis começa a ser entendida de forma mais ampla dentro da dermatologia.
Não como um ativo isolado,
mas como parte de uma estratégia que envolve:
- diferentes canabinoides
- múltiplos alvos moleculares
- formas farmacêuticas específicas
- e combinações (blends) capazes de atuar de forma complementar
Essa complexidade não é um obstáculo é o que sustenta o potencial terapêutico.
Hoje, a dermatologia já começa a incorporar essas abordagens com mais precisão, apoiada por uma ciência que vem sendo desenhada de forma cada vez mais consistente.
Não estamos diante de uma única molécula com um único efeito,
mas de um sistema expandido, integrado e altamente regulado.
Se entendemos que os canabinoides atuam em múltiplos receptores distribuídos pela pele, surge uma questão prática inevitável: como garantir que essas moléculas cheguem, de fato, onde precisam agir?
É aqui que a biotecnologia se torna parte essencial da conversa.
Canabinoides como o CBD e o CBG são altamente lipofílicos, o que, por um lado, favorece sua interação com estruturas celulares, mas, por outro, dificulta sua penetração através da barreira cutânea quando utilizados em formulações convencionais.
Não basta ter a molécula certa.
É preciso entregá-la da forma certa.
Estratégias como nanoemulsões, sistemas lipossomais e moléculas de liberação controlada vêm sendo desenvolvidas justamente para otimizar essa entrega, aumentando a permeação, a estabilidade e a biodisponibilidade dos canabinoides na pele. Na prática, isso muda completamente o resultado clínico.
A mesma molécula pode ter comportamentos diferentes dependendo da tecnologia envolvida na formulação.
E é nesse ponto que a cannabis deixa de ser vista apenas como um insumo natural e passa a ocupar um espaço dentro da biotecnologia aplicada, onde ciência, formulação e fisiologia caminham juntas.
No fim, talvez a psoríase nos ensine algo maior do que apenas sobre a pele.
Ela mostra o que acontece quando um sistema perde a capacidade de se regular.
E a ciência, aos poucos, começa a responder não apenas com bloqueios, mas com modulação.
A cannabis entra exatamente nesse ponto.
Não como solução simplificada, não como tendência,
mas como parte de uma linguagem biológica que o próprio corpo já reconhece.
Entre moléculas, receptores e sistemas, o que se desenha não é uma resposta única, mas uma nova forma de pensar o tratamento.
Mais integrada.
Mais precisa.
Mais próxima da própria fisiologia.
E talvez seja isso que mude a pergunta daqui pra frente:
não mais “o que usar na pele”,
mas “como devolver à pele a capacidade de se equilibrar”.